第一條 加快實施創新驅動發展戰略
支持深圳建設人工智能、生命信息與生物醫藥實驗室等重大創新載體,探索建設國際科技信息中心和全新體制的醫學科學院。探索知識產權證券化,規范有序建設知識產權和科技成果產權交易中心。支持深圳實行更加開放便利的境外人才引進和出入境管理制度,允許取得永久居留資格的國際人才在深圳創辦科技型企業、擔任科研機構法人代表。
第二條 加快構建現代產業體系
大力發展戰略性新興產業,在未來通信高端器件、高性能醫療器械等領域創建制造業創新中心。開展市場準入和監管體制機制改革試點,建立更具彈性的審慎包容監管制度,積極發展智能經濟、健康產業等新產業新業態,打造數字經濟創新發展試驗區。
第三條 提升教育醫療行業發展水平
探索建立與國際接軌的醫學人才培養、醫院評審認證標準體系,放寬境外醫師到內地執業限制,先行先試國際前沿醫療技術。


第七條 放寬國際新藥準入:
允許在粵港澳大灣區內地9市開業的指定醫療機構(港澳醫療衛生服務提供主體在珠三角9市按規定以獨資、合資或合作等方式設置醫療機構)使用臨床急需、已在港澳上市的藥品。
第四條 推進外籍人才簽證便利化:
1.支持深圳探索制定外籍"高精尖缺"人才認定標準,為符合條件的外籍人員辦理R字簽證。
12.賦予深圳外國高端人才確認函授權,探索優化外國人來華工作許可和工作類居留許可審批流程。
13.對外籍高層次人才投資創業、講學交流、經貿活動提供出入境便利。
第五條 探索外籍高層次人才居留便利和緊缺人才職業清單制度
為外籍高層次人才提供永久居留便利。制定緊缺人才職業清單,簡化外國人才來華工作手續,提高外國人才來華工作便利度。
第六條 實施高度便利化的境外專業人才執業制度
賦予深圳在有關部門指導下制定境外專業人才執業管理規定權限,明確職業條件、業務范圍等,允許具有境外國際通行職業資格的金融、稅務、建筑、規劃等專業人才按相關規定在深提供專業服務。放寬境外人員(不包括醫療衛生人員)參加各類職業資格考試的限制。
第八條 探索完善醫療服務跨境銜接機制:
探索建立與國際接軌的醫學人才培養、醫院評審認證標準體系。
(一)打造大灣區協同創新共同體
第九條 創新深港澳科技合作體制機制
與香港合作申請藥瓶評審體制機制改革試點。率先推動科研項目需要的醫療數據和血液等生物樣品在深港澳高校、科研機構跨境使用,探索樣品、試劑快速通關機制。
(二)促進科技創新能力同步躍升
第十條 建設國際一流的重大科技基礎設施集群
聯合大灣區優勢科研力量,建設一批重大科技基礎設施,打造空間分布上集聚、研究方向上關聯的國際一流重大科技基礎設施群。
第十一條 共建世界一流科研機構
推動深港新藥臨床試驗國際多中心基地、國家生物創新藥物技術評審機構和臨床應用新技術試驗基地等重要平臺建設。
(三)營造一流科技創新環境
第十二條 擴大科技領域對外開放
依托深圳國家基因庫發起設立"一帶一路"生命科技促進聯盟。

第十三條 推動生命經濟跨越發展:
聯合港澳重點院校和科研機構,共同發起生命健康領域大科學計劃,高標準推進國家生物產業基地建設,集中布局生物醫藥高端產業鏈、創新鏈,建設國家生命健康產業創新示范區。建立多層次基礎支撐和共性技術平臺,突破藥物研發關鍵技術,提高原研藥、首仿藥和新型制劑的創新能力,加快建設粵港澳大灣區生物醫藥國際產業帶。構建醫療器械協同創新體系,大力發展高端醫藥器械設備。著力發展精準醫療,提供基因檢測技術水平和加快個體化醫療臨床應用。
第十四條 推動大灣區海洋經濟聯動跨越發展
第十五條 構建深港澳海洋科技協同創新體系
積極構建粵港澳大灣區陸海大數據中心。
第十六條 密切粵港澳醫療衛生交流合作
吸引港澳醫療衛生服務提供主體在深設置醫療機構,探索組建粵港澳大灣區區域醫療聯合體、區域性醫療中心和專科聯盟,建立粵港澳大灣區傳染病防控機制,推動粵港澳大灣區醫療衛生信息共享平臺建設。建立與國際接軌的專科醫師培養及認證制度。
第十七條 推動粵港澳中醫藥創新發展
深化與港澳中藥檢測機構的合作,共建國際認可的中醫藥產品質量標準。推動優化港、澳中藥產品進入內地審批流程。聯合港澳一批重點大學開展現代中醫創新研究。 加快推進粵港澳大灣區中醫藥研產融合創新中心建設,打造成為集中藥產品研發、技術創新、成果轉化、標準升級、產業服務、應用示范的綜合創新平臺。
第十八條 加強深港澳食品藥品安全合作:
第十九條 打造引領世界的創新型產業集群
積極創建國家生物醫藥創新政策試驗區,爭取設立國家藥品審評中心和醫療器械審評中心粵港澳分中心,提供藥品醫療器械上市審批注冊"一站式"服務,準許香港自注冊國內尚未注冊的國際新藥、新醫療器械在合作區拓展性使用和開展臨床試驗,全面推進精準醫療、數字生命等應用示范。
第二十條 先行先試建設國家離岸創新特區
爭取在深方區域內適用保稅政策,對于科技研發設備入境免于強制性產品認證,對于科研生產需要的樣品、試劑、耗材等物資實行目錄備案制管理,予以通關便利。
第二十一條 全力推進重大科技裝置群建設
建設一批重大科技基礎設置,爭取新引進一批已列入國家重大規劃、具有稀缺性的國家設施。
第二十二條 大力推進基礎研究工作
大力支持重大研究機構建設,形成源頭創新的戰略支持。
第一條:加快深圳市生物醫藥產業高質量發展,著力提升產業原始創新能力及成果轉化。
第二條:適用于在深圳市注冊、具備獨立法人資格的從事藥品和醫療器械研發等機構。
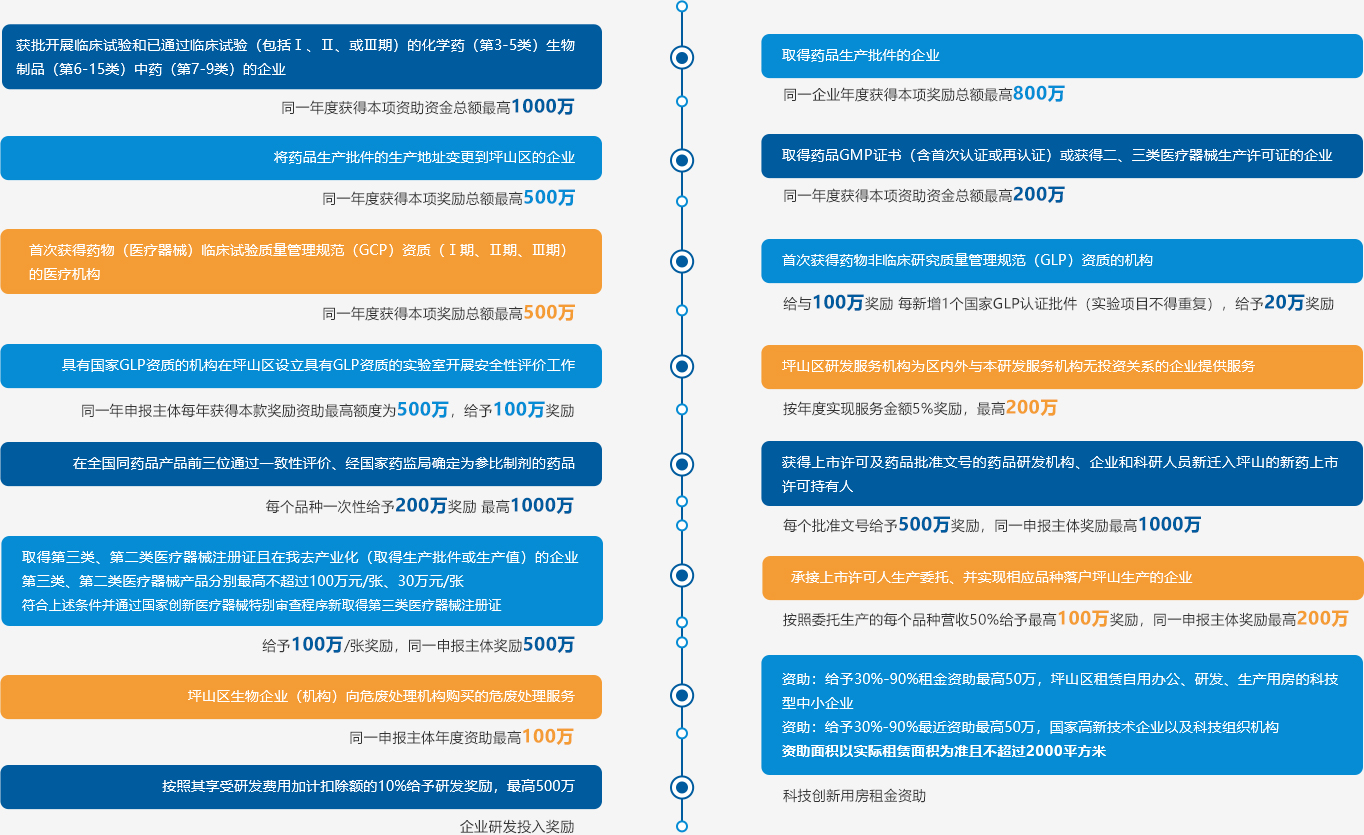
第三條
![]()
![]()
![]()
第四條
對在全國前三個通過仿制藥一致性評價的藥品,按實際投入一致性評價費用的20%予以資助,最高不超過500萬元;單個企業每年資助最高不超過1000萬元。
第五條
取得醫療器械注冊證的第二、三類醫療器械產品,按實際投入研發費用的40%予以資助,第二、三類醫療器械產品分別最高不超過300、500萬元,單個企業每年資助最高不超過1000萬元。
第六條
對我市生物醫藥企業按照MAH、醫療器械注冊人制度承擔生產的,按實際投入費用的20%予以資助,每個品種最高不超過1500萬元,單個企業每年資助最高不超過3000萬元。
第七條
對通過世界衛生組織(WHO)等國際權威認證的藥品和醫療器械,按經審計費用予以資助,最高不超過1000萬元。對通過開展國際聯合臨床研究取得境外上市的藥品,按實際投入費用的40%予以資助,最高不超過1000萬元。
第八條
對符合國家藥物臨床試驗質量管理規范(GCP)或取得國際知名認證的機構,按照項目總投資的不同百分比予以資助,最高不超過500萬元。
第九條
集聚全球頂尖科學團隊在合成生物學、腦科學、精準醫學影像等領域加快建設重大科技基礎設施,項目建設及運營經費從市政府投資中列支。
第十條
支持有望解決重大臨床需求和市場需求的新藥、高端醫療器械新技術突破,對其前期研究予以全額資助,最高不超過3000萬元;聚焦高端醫療器械、創新藥物研發等共性關鍵技術攻關,解決"卡脖子"問題,按項目總投資的40%分階段給予資助,最高不超過3億元。
第十一條
加快引進行業龍頭CRO C(D)MO 藥物毒理的研究等生物醫藥產業應用與服務基礎平臺,按項目總投資的40%予以資助,最高不超過5000萬元。
第十二條
加快建設深圳仿制藥質量與療效一致性評價技術與標準研究平臺等第三方檢測服務平臺,按實際項目總投資的40%分年度給予支持,最高不超過3000萬元。
第十三條
鼓勵醫療機構聯合粵港澳大灣區高校、科研機構等在深港科技創新合作區組建深港國際臨床醫學研究中心,開展新技術開發和應用研究等。
第十四條
積極爭取設立藥品、醫療器械審評中心(CDE)粵港澳分中心,推動生物醫藥產業創新發展。
第十五條
支持園區或園區內企業建設藥物篩選、成藥性評價、GLP實驗室等公共服務平臺,按總投資的40%予以資助,最高不超過1000萬元。
第十六條
對投資額超過20億元或可填補產業鏈空白、經濟和社會效益特別突出的重大生物醫藥產業項目,經市政府審定同意后予以重點支持。
第十七條
對符合條件的生物醫藥機構和企業,按其實際繳納保費的50%予以資助,單個保單最高不超過50萬元,單個企業每年資助最高不超過500萬元。